|
Nippon
Shokuhin Kagaku Kogaku Kaishi Vol.49, No.7, 437〜446(2002)〔総説〕
総 説
製塩法と塩の品質
橋 本 壽 夫
Processes
of Salt Manufacture and Quality of Salts
Hashimoto
Toshio
(財)ソルト・サイエンス研究財団事務理事(〒106-0032東京都港区六本木7-15-14)
The Salt Science Research Foundation, 7-15-14 Roppongi, Minatoku, Tokyo, 106-0032
1. は じ め に
塩の専売法が廃止されてから,様々な塩が販売されるようになった.専売時代には日本海水学会誌(前身は日本塩学会誌)を除いて製塩や塩に関する情報はほとんどなかった.現在でもこれらの情報は少
なく1)〜5),マスメディアや特殊製法塩の製造者の多くは,科学的根拠が乏しかったり,ないにもかかわらず,ある種の塩を誇大に宣伝して,消費者に誤った認識を与えている.
塩には家庭で使われる小物商品から,食品工場で大量に使われる商品まで様々な種類がある.用途によって塩に要求される品質,価格は異なる.家庭用であれば品質に多少のバラツキがあり価格が高くても容認されるであろうが,食品工業では品質にバラツキがなく,安い価格で安定して入手できることが重要となる.
塩の品質は製造法によって大きく影響される.製塩法と塩の品質の関係が理解されれば,塩を選定する際に役立つものと考える.
2. 製 塩 法 の 種 類
一般的に海水,塩湖水,地下塩水を濃縮する製塩法にはいろいろな種類がある.濃い塩水であるかん水を作る方法(採かん法)と,そのかん水をさらに蒸発させて塩を析出.採取する方法(せんごう法)との組合せで塩の製造法は様々に変わり,製造される塩の品質も変わる.
日本では海水を原料として製塩しているが,後述するように海水を濃縮する方法が変わってきた.また輸入された天日塩を原料にした製塩法も行われている.海外では岩塩を原料にした製塩法が一般的である.天日塩や岩塩を溶解精製して得たかん水をせんごうする方法にも真空式,加圧式,平釜式蒸発法などがある.
2.1 天日製塩法
降雨量が少なく,蒸発量が多い地域では,海水を原料として太陽熱と風力を利用して天日濃縮し,直接塩が収穫できる天日製塩法が大々的に行われている.主な生産国はメキシコ,オーストラリア,フランス,スペイン,インド,中国などである.
海水を濃縮すると溶解度の小さい塩類から順に析出してくる.その様子を図1に示した6).100 mlの海水を1/10まで濃縮,つまり10倍の濃度になるまで濃縮したとき初めて塩は析出し始める.それまでに炭酸カルシウムは100%析出し,硫酸カルシウムは80%程度析出する.硫酸カルシウムの場合は,塩化ナトリウムの析出が始まっても析出はまだ続いているので,不純物として混入してくる.さらに濃縮がすすむと硫酸マグネシウムが析出して塩の品質が悪くなる.したがって,硫酸マグネシウムの析出前に残された液をニガリとして排出して塩を収穫する.
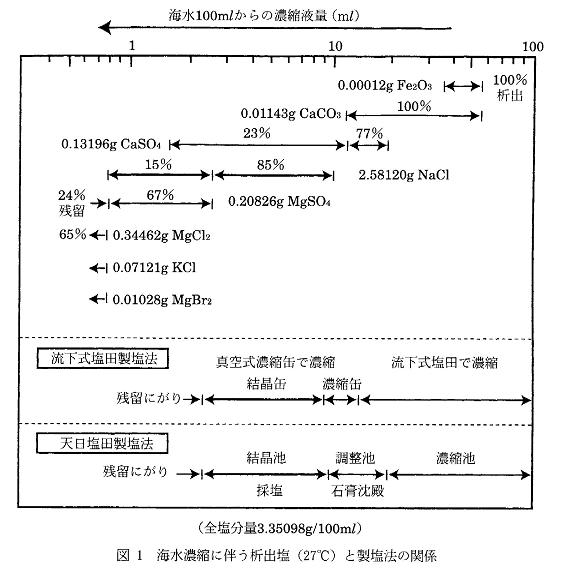
図1下部に日本の流下式塩田製塩法,海外の天日塩田製塩法の工程を付記した.流下式塩田製塩法では流下式塩田で海水を4, 5倍程度まで濃縮し,得られたかん水を真空式濃縮缶で濃縮し,結晶缶で煮詰めて塩を収穫する.
天日塩田製塩法では,海水を濃縮池に取り入れ蒸発濃縮させ,その後,調整池に移してそこでできるだけ石膏(硫酸カルシウム)を析出させる.塩化ナトリウムの飽和に近いかん水を結晶池に入れて塩化ナトリウムを析出させ,硫酸マグネシウムが析出する前にニガリを排出して塩を収穫する.海水を取り入れてから塩を収穫するまでに2年間も要する塩田から,雨期があるために数ヶ月間で塩を収穫しなければならない季節稼働の塩田まである.
2.2 イオン交換膜濃縮製塩法
イオン交換膜透析法はアメリカで薄い塩水を脱塩して飲用水を作る技術として開発された.日本ではその技術を逆用して海水濃縮のためのイオン交換膜濃縮製塩法が開発された.流下式塩田で海水を濃縮していた部分をイオン交換膜電気透析法による濃縮法に置き換えた方法である.この原理は,図2に示すように陽イオンを通す陽イオン交換膜と陰イオンを通す陰イオン交換膜を交互に並べ,陽イオン交換膜と陰イオン交換膜で形成された室内の1室おき(脱塩室)に海水を流し,両端に電圧をかけ直流電流を流すと,海水は25-30%ほど脱塩され,脱塩室で挟まれた濃縮室に塩類が18-20%の濃度で濃縮され,かん水ができる.このかん水を真空式蒸発缶で煮詰めて塩を採る.
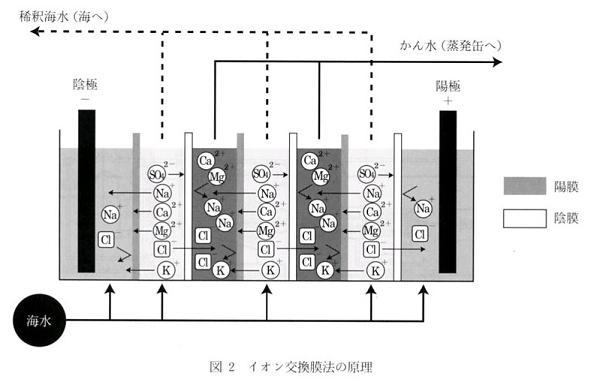
濃縮かん水の特徴は,イオン交換膜の性質によってスケール成分となるカルシウムと硫酸イオンが少なくなることと,カリウムが多くなることである.したがって,そのかん水を濃縮すると,溶解度の関係で析出する塩類は図3に示す順に析出してくる7).ここでも硫酸カルシウムと塩化ナトリウムは平行して析出するが,シックナーで分離される.製塩の終点は塩化カリウムが析出する直前である.
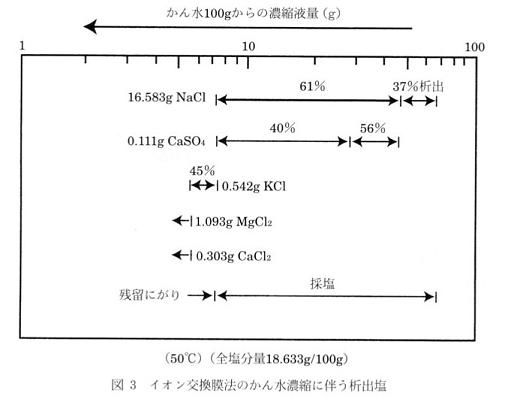
イオン交換膜濃縮製塩法では全面的に化石エネルギーを使う.エネルギー利用効率を高めるために,図4に示すように自家発電と発電排蒸気を真空式蒸発缶の熱源に利用するコゼネレーション方式が採用されている8).すなわち,透析電力と蒸発装置その他の運転に必要な電力や照明電力を自家発電で賄い,排蒸気を4重効用の真空蒸発缶で利用するので,非常に熱効率の良い設備となっており,生産コストの低減に大きく寄与している.
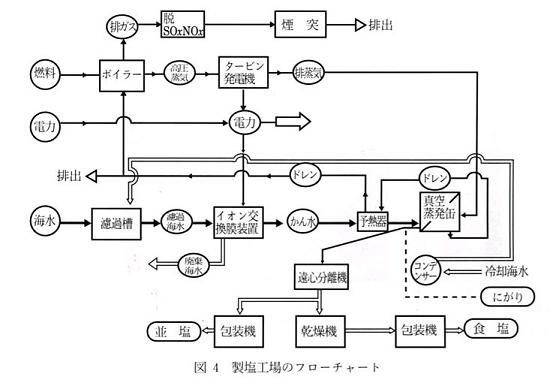
2.3 天日塩の溶解再製製塩
輸入された天日塩を溶解し,カルシウム,マグネシウムを出来るだけ除去するかん水精製工程を経て真空式蒸発缶でせんごうする製塩法である.食卓塩,精製塩などがこれに当たる.天日塩を溶かしてろ過し異物を除去した後,平釜でせんごうする製品もある.天日塩を原料とした多くの特殊製法塩がこれに当たる.
2.4 岩塩の溶解再製製塩
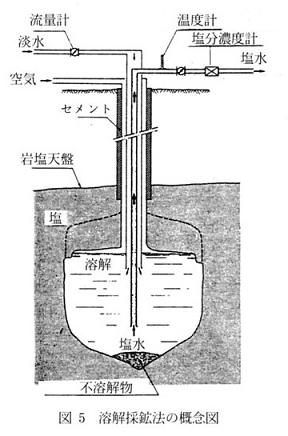
外国のせんごう塩の大部分は岩塩を溶解したかん水を精製(カルシウム,マグネシウムイオンを除去)して,真空式または加圧式蒸発缶で煮詰め直して製造する.基本的には天日塩の溶解再製塩と同じ品質の塩となる.岩塩の溶解は図5に示すように,岩塩層に水を注入して塩を溶かしてかん水として汲み上げる方法で行われる9).塩が溶解した後の空洞のために地盤が沈下して災害を起こさないように,絶えず空洞の形状を認識しながら溶解採鉱を進める.
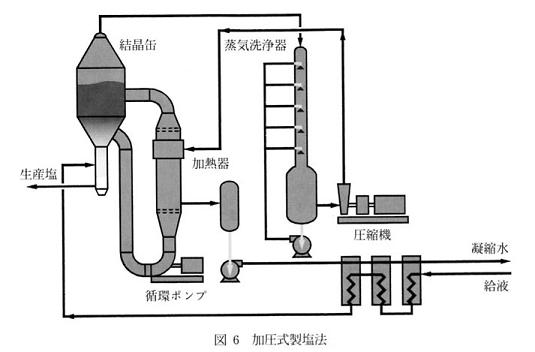
加圧式蒸発法は電力の安いヨーロッパでよく使われている.昭和27年から10年間ほど日本でも加圧式蒸発缶で海水直煮せんごう法による製塩が行われていた.図6に示すように蒸発缶で発生した蒸気は,飛沫同伴された塩分を除くために蒸気洗浄機で洗浄され,圧縮機で圧縮加圧され高温の蒸気となって蒸発缶の加熱器に供給される10).
2.5 平釜式製塩法
昭和になってから真空蒸発缶による製塩が始まったが,戦後の昭和20年代までは平釜式のせんごう法が続いていた.熱効率の悪さと少量生産にしか対応できないことから使用されなくなった.昭和47年に国内製塩がイオン交換膜製塩法に全面転換してから特殊用塩の製造法として天日塩を溶解したかん水を煮詰めるために平釜が使われるようになった.塩専売制が廃止され,届け出で海水から塩を製造できるようになってから平釜式で製造される塩が多くなった.
アメリカではアルバーガ一法11)と称する平釜式せんごう法で大量の塩を製造している工場がある.この方法は別の加熱器で加熱されたかん水を平釜に注ぎ,液表面で蒸発させることを特徴としている.
2.6 粉砕節別
岩塩や天日塩を粉砕・篩い分けして粒径を揃えて製品とする.通常,岩塩は純度的に品質が悪く,道路の融氷雪剤として使われる場合が多いが,稀な例として非常に純度の高い岩塩もあり,そのような岩塩は食用としても使われる.
2.7 圧縮加工成型
せんごう塩や粉砕塩をペレット状,アーモンド状,板状,大きな塊に機械で圧縮成型して塩製品を作る.
3. 塩 の 品 質
塩の品質を考えるとき,昧の問題に関連した要因としては化学組成や溶解速度があり,用途や取り扱い上の問題には物性が大きく関連してくる.表1には塩事業センター(旧日本たばこ塩専売事業本部)の塩の規格を示した.
| 表1 塩事業センターの塩の規格 |
| 種 類 |
品 質 規 格 |
|
|
備考(生産方法) |
|
純 度 |
粒 度 |
添 加 物 |
| 食卓塩 |
NaCl 99%以上 |
500〜300μm 85%以上 |
塩基性炭酸マグネシウム基準0.4% |
原塩(天日塩)を溶解し再製加工した物 |
| ニュークッキングソルト |
同上 |
同上 |
同上 |
同上 |
| キッチンソルト |
同上 |
同上 |
同上 |
同上 |
| クッキングソルト |
同上 |
粒度500〜180μm 85%以上 |
同上 |
同上 |
| 特級精製塩 |
NaCl 99.8%以上 |
同上 |
|
同上 |
| 精製塩1kg |
NaCl 99.5%以上 |
同上 |
塩基性炭酸マグネシウム基準0.3% |
同上 |
| 精製塩25kg |
同上 |
同上 |
|
同上 |
| 新家庭塩 |
NaCl 90%以上 |
600〜150μm 80%以上 |
|
イオン交換膜海水濃縮法によるかん水を煮詰めた物 |
| 食塩 |
NaCl 99%以上 |
同上 |
|
同上 |
| 並塩 |
NaCl 95%以上 |
同上 |
|
同上 |
| つけもの塩 |
同上 |
|
リンゴ酸基準0.05% クエン酸基準0.05% 塩化マグネシウム0.1% 塩化カルシウム規準0.1% |
洗浄した粉砕塩に添加物を加えた物 |
| 原塩 |
同上 |
|
|
外国から輸入した天日塩 |
| 粉砕塩 |
同上 |
|
|
原塩(天日塩)を粉砕したもの |
3.1 組成
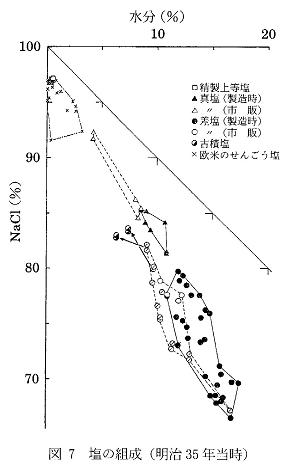
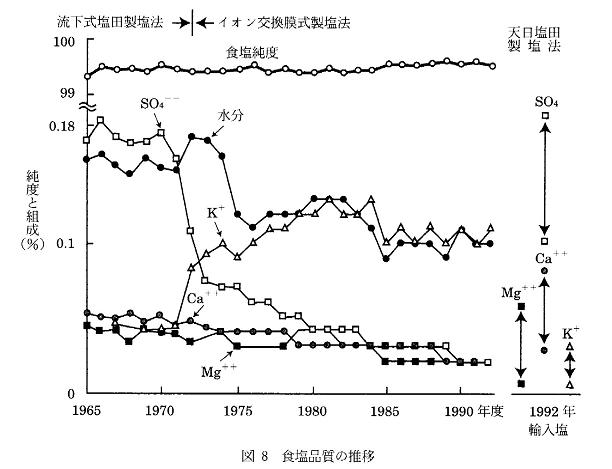
塩専売制度が廃止されてから,海水を原料としていろいろな塩製品が市場に出てきた.塩専売制が施行される前の塩の純度は図7に示す状態であり12),専売制開始後の変遷は表212)に示す通りであった.日本の製塩法が昭和36年頃からイオン交換膜による採かん法に変わり始め,47年に全面転換されてから塩の組成は現在のように変わった.その前後の様子を図8に示す6).濃縮かん水に特徴があるので,製品品質も組成的に塩田製塩時代の塩とは少し異なる.これには天日塩の組成も示されている.2年間もかけて海水をゆっくりと濃縮させる塩田で製造された天日塩は緻密な結晶となるため,純度の高い品質の塩となる.逆に,季節稼働のために数ヶ月間で収穫される塩は急速に結晶成長をさせるために,結晶内にかん水が閉じ込められ純度が悪くなる.
| 表2 国内塩純度の推移 |
| NaCl純度% |
|
70 |
|
75 |
|
80 |
|
85 |
|
90 |
|
95 |
|
|
5等 |
|
4等 |
|
3等 |
|
2等 |
|
1等 |
|
| 明治38年 |
|
55.5 |
|
21.4 |
|
15.1 |
|
4.5 |
|
0.6 |
|
| 大正 9年 |
|
40 |
|
|
|
45 |
|
|
|
|
|
| 15年 |
|
|
|
|
|
86.6 |
|
12.3 |
|
|
|
| 昭和 4年 |
|
|
|
|
|
|
|
50%を越える |
|
|
|
| 10年 |
|
0.1 |
|
- |
|
27.7 |
|
60.8 |
|
11.4 |
|
| 12年 |
|
0.1 |
|
0.1 |
|
12.2 |
|
60.3 |
|
27.3 |
|
| 13年 |
|
0.1 |
|
0.1 |
|
10.4 |
|
69.3 |
|
21.1 |
|
| 15年 |
|
等外 0.1 |
|
|
|
並塩 75.6 |
|
上等 24.3 |
| |
|
|
|
|
|
平釜、その他 |
|
蒸気利用 |
|
加圧式、真空式 |
|
| 20年 |
|
|
|
|
|
31.9 |
|
27.2 |
|
40.9 |
|
| 25年 |
|
|
|
|
|
9.5 |
|
34.0 |
|
56.5 |
|
| 29年 |
|
|
|
|
|
8.7 |
|
16.7 |
|
74.4 |
|
上質塩 2.0 |
| 国内塩の純度別生産比率 (%) |
| (注) 1) 明治38年塩専売施行に当たり、NaCl%による等級を規定。 |
| 2) 大正11年を境としてそれまでの4,5等塩中心から3等塩が中心となる。 |
| 3) 昭和15年1月等級改正。 |
| 4) 昭和20年以降せんごう方式別に品質規格を定めた。 |
| 5) 昭和29年上質塩(純度95%以上、紙袋)生産開始。 (元の表より抜粋) |
塩専売制が廃止されてから国内でも様々な塩が作られ,外国からもいろいろな塩が輸入されて市販されている.日本たばこ(株)から業務を引き継いだ(財)塩事業センターでは主立った製品を分析して発表した13).それによるとFAO/WHO合同規格案作りで検討されている食用塩の国際規格(案)で有害汚染物となっている成分も検出されている製品がある.ちなみに案で指定されている有害汚染物と濃度はいずれも単位がppm以下となっており,具体的な数値はヒ素が0.5,銅が2,鉛が2,カドミウムが0.5,水銀が0.1である.
東京都でも消費者の問い合わせに応えるために商品のキャッチフレーズを整理し,組成を分析し,調理に塩を用いて味覚テストをした結果を商品テスト・シリーズ(9-3)として冊子14)にまとめ関係機関に配布した.テストの結論を簡潔に述べると誇大宣伝の商品が多く,表示の改善を望むものであった.
特殊製法塩中にはミネラルが多く,ミネラル摂取量に期待を持たせるような表示がされていることがある.塩からのミネラル摂取量を表3に示した6).一日必要量と10 gの塩を作るために必要な400 mgの海水中の含有量と比較すれば,塩からナトリウム以外のミネラル摂取を期待できないことがわかる.
| 表3 塩からのミネラル摂取量 |
| 元素 |
一日必要量 |
一日摂取量 |
|
食塩10 g中の量 |
|
海水100 ml中の量 |
海水組成のままで作った塩10 g中の量(海水として約400ml) |
|
|
|
昭和11年 |
昭和37年 |
昭和59年 |
|
|
|
|
(国内塩) |
(食塩) |
(食塩) |
|
| カルシウム |
600 mg (所要量)* |
531 mg (平成2年度) |
38 mg |
9 mg |
3 mg |
40 mg |
160 mg |
| リン |
Caとほぼ当量* |
|
|
|
|
0.002 mg |
0.008 mg |
| カリウム |
2-4 g (目標摂取量)* |
|
21 mg |
6 mg |
13 mg |
38 mg |
152 mg |
| ナトリウム |
3.9 g (目標摂取量)* |
5 g (平成2年度) |
3.77 g |
3.91 g |
3.98 g |
1.05 g |
3.93 g |
| マグネシウム |
300 mg (目標摂取量)* |
|
50 mg |
7 mg |
3 mg |
135 mg |
541 mg |
| 鉄 |
10 mg (所要量)* |
10.9 mg (昭和58年度) |
|
|
0.0017 mg 以下 |
0.0005 mg |
0.002 mg |
| 亜鉛 |
10 mg程度* |
6-27 mg |
|
|
0.0012 mg以下 |
0.001 mg |
0.004 mg |
| 銅 |
1-3 mg |
0.78-4.7 mg |
|
|
0.0006 mg以下 |
0.0003 mg |
0.001 mg |
| クロム |
0.29 mg |
0.18-3.32 mg |
|
|
|
0.000005 mg |
0.00002 mg |
| ヨード |
0.1-0.14 mg |
1-4 mg |
|
|
0.004 mg以下 |
0.006 mg |
0.02 mg |
| コバルト |
0.02-0.16 mg |
0.002-0.045 mg |
|
|
|
0.00001 mg |
0.00004 mg |
| セレン |
0.03-0.06 mg |
0.1-0.2 mg |
|
|
|
0.00004 mg |
0.0002 mg |
| マンガン |
0.7-2.5 mg |
5.5-10.4 mg |
|
|
|
0.0002 mg |
0.0008 mg |
| モリブデン |
0.1 mg |
0.15 mg |
|
|
|
0.0006 mg |
0.002 mg |
| * 第四次改訂日本人の栄養所要量より |
3.2 物 性
塩の物性により塩の用途が決まることが多い.塩を取り扱う上でも物性が大きな問題となる.塩の物性には比重,硬度,溶解度といった学術的な性質もあるが,用途から実用上問題となるのは嵩比重(嵩密度),結晶の壊れ易さ,溶解速度,流動性,付着性,といったことである.これらの性質はお互いに関連しあっており,ひとつの物性が変わるとそれに伴って他の物性も変わる.物性に大きな影響を及ぼす要因は結晶形状と粒度分布である.
3.2.1 結晶形状
塩の形は図9に示すように塩の結晶成長の様子で変わることが村上により報告されている15).通常,真空蒸発缶などで大量に生産される300-500 μmサイズの塩はほぼ立方体状である.粒径が大きくなったり,流動状態が変わることにより結晶成長中に角が取れて丸い球状の塩になる.平釜を使い液表面上で結晶成長させるとピラミッド状,またはホッパー型の塩ができ,厚さの薄い鱗片状のフレーク塩となる.平釜を使い液中で結晶成長させると,立方体結晶が多数凝集した状態で成長するので無定形となり,ザクザクした手触りの粗塩となる.天日塩や岩塩を粉砕した製品でも無定形となり,ザクザクした手触りの塩となる.
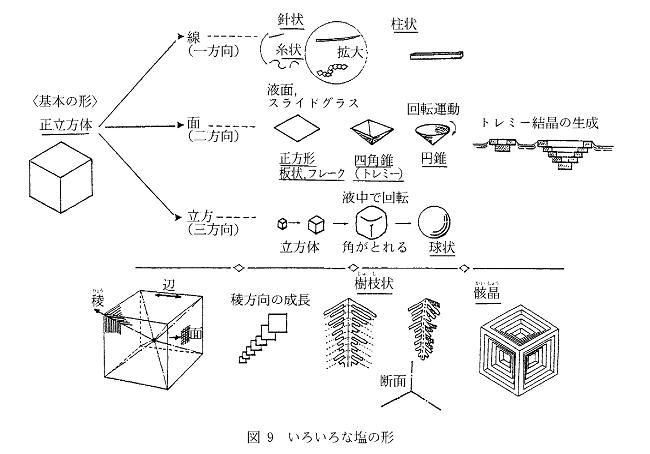
形が塩の物性に及ぼす影響は大きい.流動性は塩の取り扱い上重要な物性である.食卓塩のように振出容器から出して使う場合には流動性が良くないと詰まってしまい細孔から振り出せない.固形の塩が口に入るような料理の場合には,塩の溶け易さにより塩味や風味が変わる.フレーク塩のように壊れやすく溶け易いことや嵩密度が小さいことも重要な物性となる.例えば,ごまと塩を混合したごま塩では塩の嵩密度をごまの嵩密度と同じようにしないと均一に混合しない.付着性も嵩密度と関係しており,嵩密度が小さくないと付着性が悪い.
3.2.2 粒度分布
粒径が大小,サイズが揃っているかどうかも重要な物性の一つである.これにより流動性,付着性,溶解性,嵩密度などが変わってくる.
3.3 添加物
塩の添加物としては,調味料,天然物(胡椒,ごま等),ミネラル(カルシウム,マグネシウム等)などがあり,これらの添加により塩の組成は変わることから塩の味や風味が変わる.また塩基性炭酸マグネシウムなどの添加により塩の固結防止や流動性を付与し,塩の物性を変える添加物もある.
日本の気象条件では高純度の塩は特に夏場に固結し易い.これを完全に防止するには10 ppm程度のフェロシアン化カリウムを添加すればよく,海外では一般的に使われている.しかし,日本では食品添加物に指定されていないので輸入品には注意する必要がある.
4. お わ り に
製塩法と塩の品質との関係について簡潔に述べたが,塩の機能や用途との関係については触れる紙幅がなかった.人間の食生活,生命維持に不可欠な塩であるが,安い物で身近にあって湯水のごとく使える時代になっているので,マスメディアの力もあって付加価値を付けた高価な商品に魅力を感じる.しかし,本当に価格に見合った付加価値があるのかどうか,消費者はよく考える必要がある.
引 用 文 献
1)福場博保,小林彰夫編集,調味料・香辛料の事典,塩味料 (朝倉書店,東京) p.81 (1991).
2) 日本海水学会晶析委員会,製塩工業における晶析 (化学工業社,東京) (1997).
3) 日本海水学会,(財)ソルト・サイエンス研究財団共編,塩の分析と物性測定(学会誌刊行センター,東京) (1992).
4) Kaufmann, D. W., Sodium chloride (American Chemical Society, Washington) (1978).
5) 杉田静雄,塩の科学 (海游舎,東京) (2001).
6) 橋本壽夫,Kewpie News,No. 293 (1998).
7) 橋本壽夫,調理科学,23, 138 (1990).
8) 村上正祥・藤原 滋,海水誌,34,49 (1980).
9) Le Sel, Companie des Salins du Midi et des salines de
L’est, Presses Universitaires de France (1985).
10)Hudel, G. and Karoly, J., In
Symposium on Salt, Vol.II, ed. Kakihana, H. et al.
(EIsevier, Amsterdam ) p.151 (1993).
11)久保村喜代子,食品と科学,5月号,30 (1993).
12)村上正祥,海水誌,38,236 (1984).
13)新野 靖,西村ひとみ,古賀明洋,篠原富男,伊藤浩士,日本調理科学会誌,32,133 (1999).
14)東京都消費生活総合センター,商品テスト・シリーズ (9-3) いろいろな「塩」,(1998).
15)村上正祥,海水誌,40,17 (1986).
(平成13年9月20日受理)
|